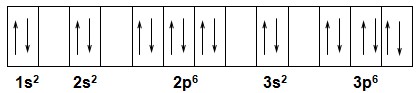
A partir dos resultados discutidos na primeira seção,
principalmente daqueles obtidos por
Lenard, Einstein desenvolveu, em 1905, uma teoria muito simples e
revolucionária para explicar o efeito fotoelétrico. Simplesmente, ao invés de considerar a
luz como uma onda, ele propôs que ela seja composta de corpúsculos, denominados fótons. Cada
fóton, ou quantum de luz, transporta uma energia dada por h
n, onde h é a constante de Planck,
e
n é a freqüência da luz. A proposta de Einstein recupera uma
idéia que foi defendida por Newton, e
abandonada depois do experimento de Young (este experimento será tratado no cap. 5).
De acordo com esta proposta, um quantum de luz transfere toda a sua energia (hf) a um
único elétron,
independentemente da existência de outros quanta de luz. Tendo em conta
que um elétron ejetado do interior do corpo perde energia até atingir a
superfície, Einstein propôs a seguinte equação, que relaciona a energia do
elétron ejetado (E) na superfície, à freqüência da luz incidente (
n) e à função trabalho do metal (
f), que é a energia necessária para escapar do
material. Isto é,
E = hn - f
A equação acima vale para todos os elétrons ejetados. Como elétrons são ejetados de diferentes
profundidades do material, tem-se uma distribuição de energia. Einstein sugeriu que se usa-se
apenas os elétrons mais energéticos, isto é, aqueles que saíssem da parte mais superficial.
Assim, a equação de Einstein transforma-se em
Emax = hn - f
Conhecendo-se E
max e a frequência da luz incidente, é possível determinar h e
f.
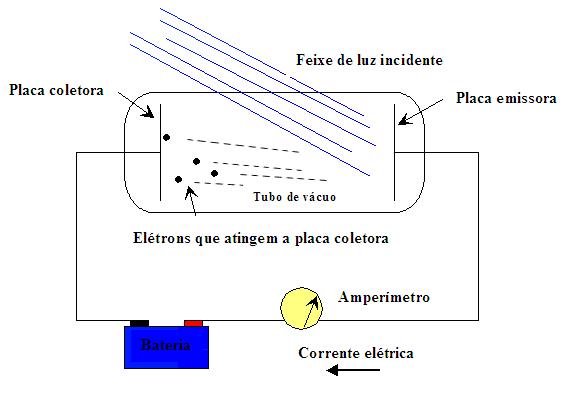
Para entender como se determina a energia cinética máxima dos elétrons, veja a ilustração do
arranjo experimental, extraída de
http://www.phys.virginia.edu/.
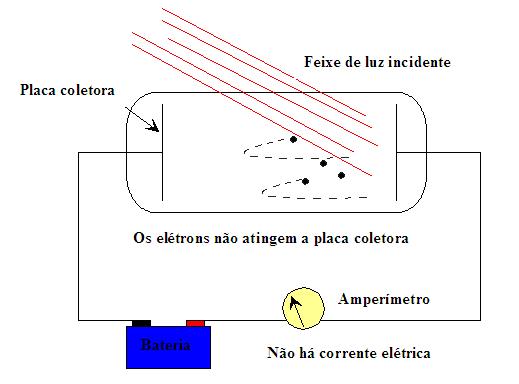
Se o potencial negativo da placa coletora for nulo, todos os elétrons que saem da placa
emissora chegam na coletora. Este é o caso em que temos a maior distribuição de fóton-elétrons.
Se aumentarmos este potencial retardador, a corrente diminui. Quando a corrente for zero, tem-se um
potencial (também conhecido como potencial de corte)
capaz de repelir os elétrons mais energéticos. Então eV é uma estimativa de E
max.
Agora podemos escrever a equação de Einstein na forma adequada para a verificação experimental:
eV = hn - f
A equação acima pode ser escrita de uma forma ainda mais apropriada:
V = hn - f
Neste caso, V é dado em volts, h em ev.s,
n em Hz e
f em eV.
A partir da sua equação, Einstein fez a seguinte proposta para ser verificada experimentalmente:
variando-se a freqüência,
n, da luz
incidente e plotando-se V
versus n, obtêm-se uma reta, cujo
coeficiente angular deve ser h/
e. Este foi o primeiro experimento que demonstrou a
universalidade da constante de Planck. Isto é, h é uma constante independente do material
irradiado. Vejamos uma simulação dessa experiência proposta por Albert Einstein.
Nesta "experiência", uma lâmpada de mercúrio é usada para produzir a luz incidente. Esta lâmpada
é vista na parte superior esquerda da figura. Cinco linhas espectrais são filtradas, para produzir
feixes monocromáticos: amarelo, verde, violeta e dois feixes de ultravioleta. Cada linha é
caracterizada pela sua freqüência.
O catodo (placa emissora) é indicado pela letra "C", enquanto o anodo (placa coletora) é
indicado pela letra "A". A corrente fotoelétrica é medida no amperímetro (equipamento com tarja
vermelha), enquanto o potencial retardador é indicado no voltímetro (tarja azul).
O painel à direita permite que se escolha o material do catodo (césio, potássio ou sódio) e a
luz incidente. Além disso, é possível variar o potencial retardador. O resultado da "medida" é
plotado no gráfico do potencial versus freqüência, à esquerda do circuito.
Para cada catodo, há um conjunto de pontos no gráfico Vxf. Estes pontos são ajustados por uma
reta, cujo coeficiente angular fornece o valor da constante de Planck, e a interseção da reta com o
eixo vertical fornece o valor da função trabalho.
O primeiro pesquisador experimental a apresentar resultados realmente
importantes para comprovar a equação de Einstein foi Arthur
Llewellyn Hughes, que demonstrou, em 1912, que a inclinação
da função E (
n)
variava
entre 4,9x10
-27 e 5,7x10
-27 erg.s, dependendo da
natureza do material irradiado.
Em 1916,
Millikan publicou um extenso trabalho sobre seus resultados
obtidos na Universidade de Chicago. Ele comprovou que a equação
de Einstein se ajusta muito bem aos experimentos, sendo h = 6,57x10
-27
erg.s. Em 1949, Millikan confessou ter dedicado mais de dez anos de trabalho
testando a equação de Einstein, com absoluto ceticismo em
relação à sua validade. Todavia, contrariando todas
as suas expectativas os resultados experimentais confirmaram a teoria de
Einstein sem qualquer ambiguidade. Este comentário reflete muito
bem a postura da comunidade científica da época diante da
proposta de Einstein. Entre 1905 e 1923, poucos foram os que levaram a
sério sua teoria, entre os quais podemos destacar Planck.